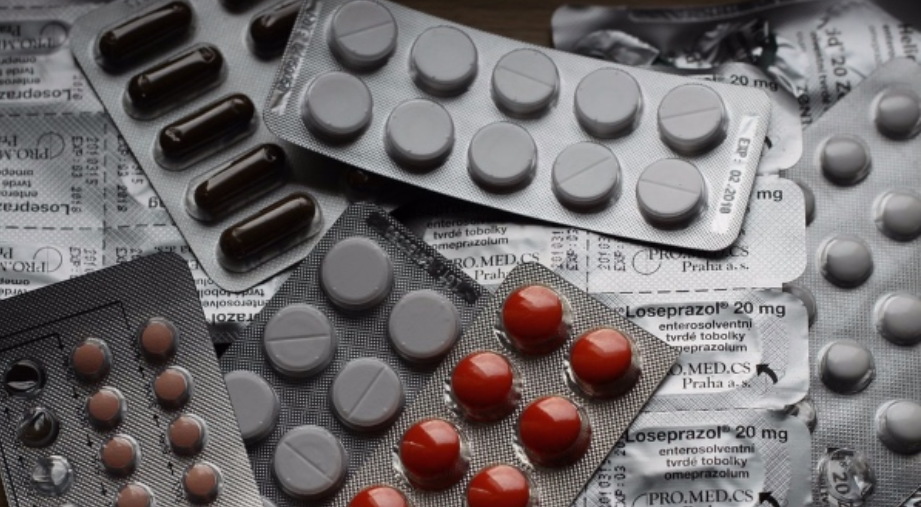
La Administración de Medicinas y Alimentos de Estados Unidos (FDA por sus siglas en inglés) dio a conocer el pasado 13 de septiembre que los medicamentos reductores de ácido contienen una impureza en niveles bajos, vinculada con partículas cancerígenas.En un informe emitido al respecto señala que el NDMA se clasifica como un probable carcinógeno humano, según las pruebas de laboratorio.El informe añade que es un contaminante ambiental conocido y se encuentra en el agua y los alimentos, incluidas las carnes, los productos lácteos y las verduras.
La FDA evalúa si los bajos niveles de NDMA en Ranitidina representan un riesgo para los pacientes.Tras la alerta, diversos laboratorios anunciaron que están deteniendo la distribución de medicamentos con Ranitidina.
“Nuestra investigación interna está en curso para determinar más detalles. En caso de inquietudes, medidas adicionales adecuadas será implementado en alineación con las autoridades de salud relevantes según sea necesario”, dijo Novartis en un comunicado.
El fabricante de medicamentos Sanofi, que elabora productos de ranitidina vendidos bajo la marca Zantac, dijo en un comunicado, enviado el jueves, que actualmente “no tiene planes de dejar de distribuir o fabricar Zantac u otros productos de ranitidina fuera de Canadá”.“La FDA informó que los niveles de N-nitrosodimetilamina (NDMA) en la ranitidina en las pruebas preliminares apenas superan las cantidades que se encuentran en los alimentos comunes.
Estamos trabajando estrechamente con la FDA y estamos llevando a cabo nuestras propias investigaciones robustas para garantizar que sigamos alcanzando los niveles más altos seguridad de calidad y estándares de calidad”, declaró el laboratorio.Se recomienda, a quienes consumen la Ranitidina recetada, hablar con sus médicos sobre otras opciones de tratamiento.